HOMEPAGE
ประเภทของสารประกอบโคเวเลนต์
ประเภทของสารประกอบโคเวเลนต์
การเกิดสารประกอบโคเวเลนต์
เกิดจากอะตอมของอโลหะทำปฏิกิริยากับอะตอมของอโลหะโดยอะตอมของอโลหะจะนำอิเล็กตรอนวงนอกมาใช้ร่วมกันเป็นคู่ ๆเพื่อให้อยู่สภาวะที่เสถียร และจะอยู่เป็นโมเลกุลชัดเจนว่า1โมเลกุลมีกี่อะตอม
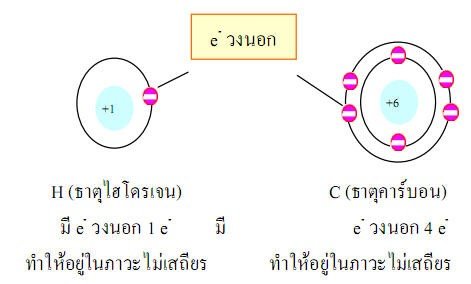

ตารางที่4แสดงความต้องการใช้อิเล็กตรอนร่วมกับอะตอมของธาตุอโลหะ เพื่อให้อยู่ในภาวะเสถียร
| ||||||||||||||||||||||||||||||||||||||||||||
|
ตัวอย่างที่1อะตอมของธาตุไฮโดรเจน 2 อะตอม รวมกับอะตอมของธาตุออกซิเจน1อะตอมได้น้ำ1โมเลกุล
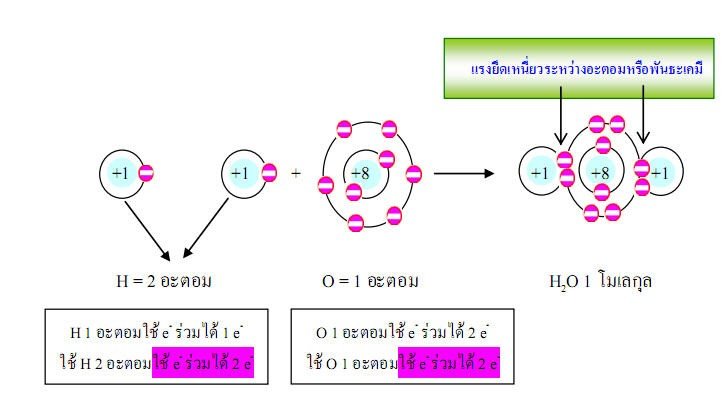
ตัวอย่างที่2อะตอมของธาตุคาร์บอน 1 อะตอม รวมกับอะตอมของธาตุไฮโดรเจน4อะตอมได้แก๊สมีเทน (CH4)1โมเลกุล
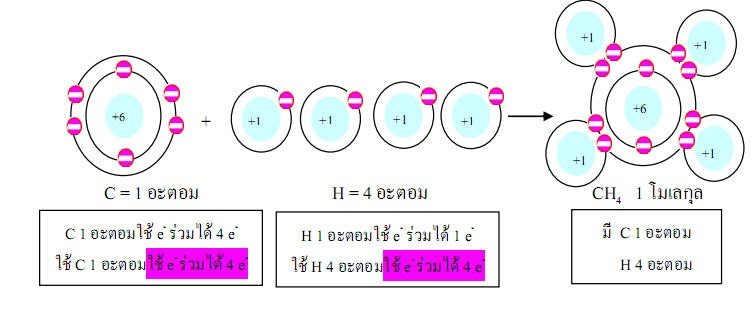
สารประกอบโคเวเลนต์ แบ่งเป็น 2 ประเภท
1. Homonuclear molecule (โมเลกุลของธาตุ) หมายถึงสารประกอบโคเวเลนต์ที่ในหนึ่งโมเลกุลประกอบด้วยอะตอมของธาตุชนิดเดียวกันมายึดกันด้วยพันธะโคเวเลนต์ เช่น H2, O2,Br2 ,N2 ,F2 ,Cl2เป็นต้น
2. Heteronuclear molecule (โมเลกุลของสารประกอบ) หมายถึง สารประกอบโคเวเลนต์ที่ในหนึ่งโมเลกุลประกอบด้วยธาตุตั้งแต่ 2 ชนิดขึ้นไป มายึดกันด้วยพันธะโคเวเลนต์ เช่น HCl , CH4, H2O , H2SO4 ,HClO4เป็นต้น
สมบัติของสารประกอบโคเวเลนต์
สารประกอบโคเวเลนต์ มีสมบัติดังนี้
|
1. มีสถานะเป็นของแข็ง ของเหลว หรือแก๊ส เช่น
|
- สถานะของเหลว เช่น น้ำเอทานอลเฮกเซน
|
- สถานะของแข็ง เช่น น้ำตาลทราย (C12H22O11),แนพทาลีนหรือลูกเหม็น (C10H8)
|
- สถานะแก๊ส เช่น แก๊สคาร์บอนไดออกไซด์ (CO2),แก๊สมีเทน (CH4),แก๊สโพรเพน (C3H8)
|
2. มีจุดหลอมเหลวต่ำ หลอมเหลวง่ายเนื่องจากมีแรงยึดเหนี่ยวระหว่างโมเลกุลที่ไม่แข็งแรงสามารถถูกทำลายได้ง่าย
|
3. มีทั้งละลายน้ำและไม่ละลายน้ำ เช่น เอทานอลละลายน้ำ แต่เฮกเซนไม่ละลายน้ำ
|
4.สารประกอบโคเวเลนต์ไม่นำไฟฟ้าเนื่องจากมีประจุไฟฟ้าเป็นกลาง และอิเล็กตรอนทั้งหมดถูกใช้เป็นอิเล็กตรอน
คู่ร่วมพันธะระหว่างอะตอม ทำให้ไม่มีอิเล็กตรอนอิสระช่วยนำไฟฟ้า แต่ยกเว้นในสารประกอบโคเวเลนส์ที่มีสภาพขั้วแรงมาก เช่น HCI, HBr, H2SO4
**แกรไฟต์เป็นรูปหนึ่งของคาร์บอนเกิดจากอะตอมของคาร์บอนสร้างพันธะโคเวเลนต์กับอะตอมที่อยู่ข้างเคียง
อีก 3 อะตอม ทำให้เกิดการยึดเหนี่ยวเป็นโครงตาข่ายเป็นชั้น ๆ มีความแข็งแรงภายในชั้นสูง ส่งผลให้แกรไฟต์
มีจุดหลอมเหลวและจุดเดือดสูง ส่วนแรงยึดเหนี่ยวระหว่างชั้นระหว่างชั้นเป็นแรงแวนเดอวาลส์ซึ่งเป็น
แรงยึดเหนี่ยวที่ไม่แข็งแรงนัก ดังนั้นแกรไฟต์จึงสามารถแตกหักและเลื่อนไหลออกเป็นชั้น ๆ ได้ง่าย
|





ไม่มีความคิดเห็น:
แสดงความคิดเห็น